�߿����W��݆�������|�ἃ���x���w�Ƃ䌣�}���Y
2019-01-07 17:46:47���þW
����һ�����|���ἃ�ͷ��x���o�C��
������һ�����������x���ἃ�Ļ���Ҫ��ԭ�����_���������㣬����ԇ���������p��(��p�ٺ���)�����o�h��?
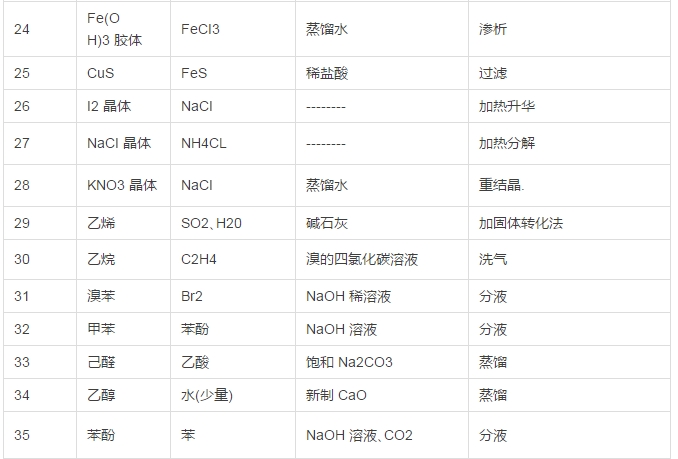
�����������������x���ἃ���õķ�������������������������P���÷��������m�������б����£�
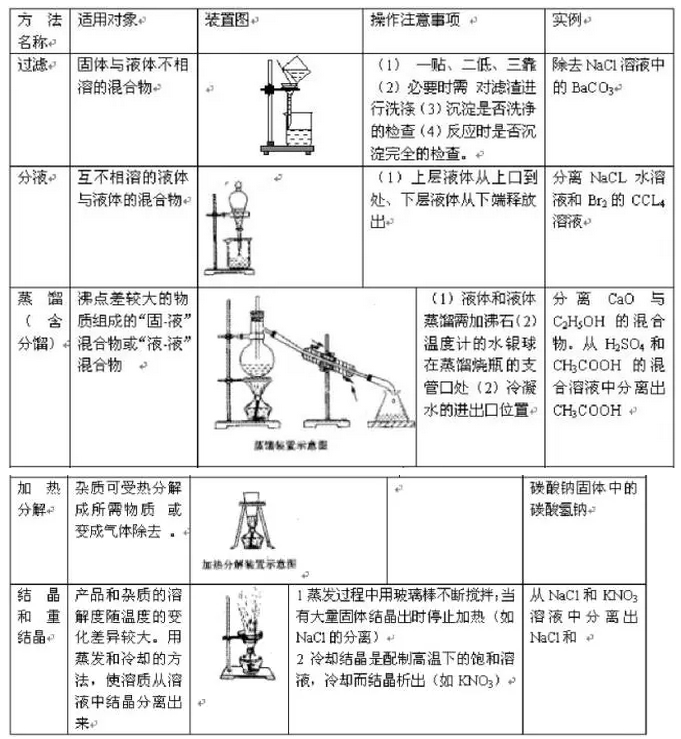

���������磺
��������(ijҺ�w)�D��������Һ�е��s�|�����D������Һ�е���Ҫ�ɷֻ���w����������ȥ�������Һ�е�̼��⛣�ͨ�^��CO2��ȥNaHCO3��Һ�е�Na2CO3��
������������������е�ij�N�M���ױ�ij�N����������������ľ̿ʹ������ҺÓȥ�ЙCɫ�ء�
��������������߀ԭ���D��������Һ�е��s�|�ױ�������߀ԭ������ɷ֣���ͨ�Ț��ȥFeCl3��Һ�е�FeCl2�����F��ȥFeCl2�е�FeCl3��
������Ҋ���|���s������
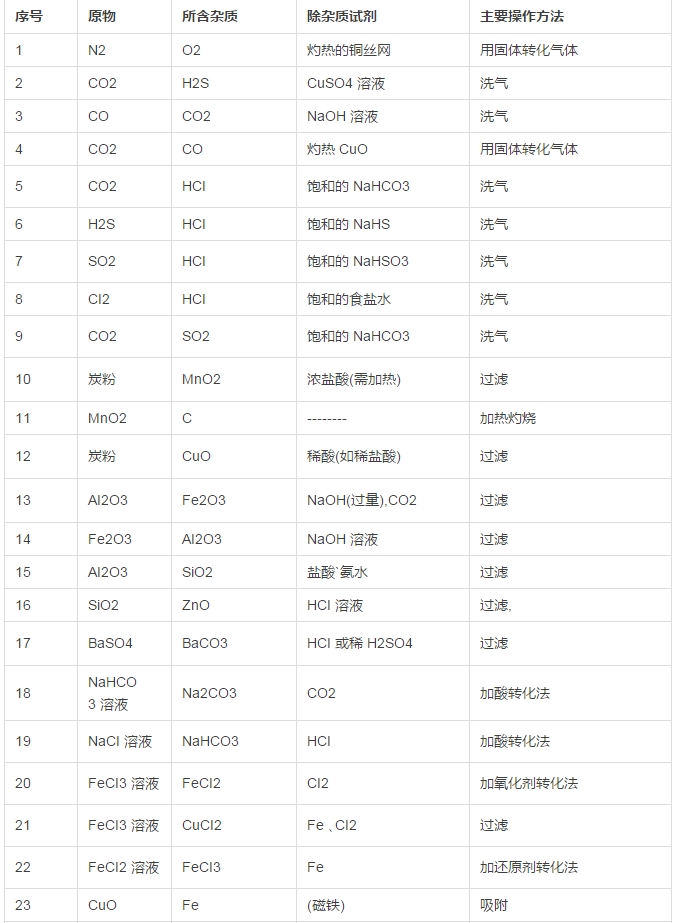
�����������w���Ƃ�
������һ�����w����b�õ��OӋ
����1���b������ƚ��b��→�����b��→�������ռ��b��→��β���b��
����2�����b����������ϣ���������
����3����������b��x��→�z������→����ˎƷ→�M�Ќ��
�������������w�l���b�õ����
����1���OӋԭ�t����������ԭ�����������B�ͷ�������l���������x���b��?
����2���b�û�����ͣ�
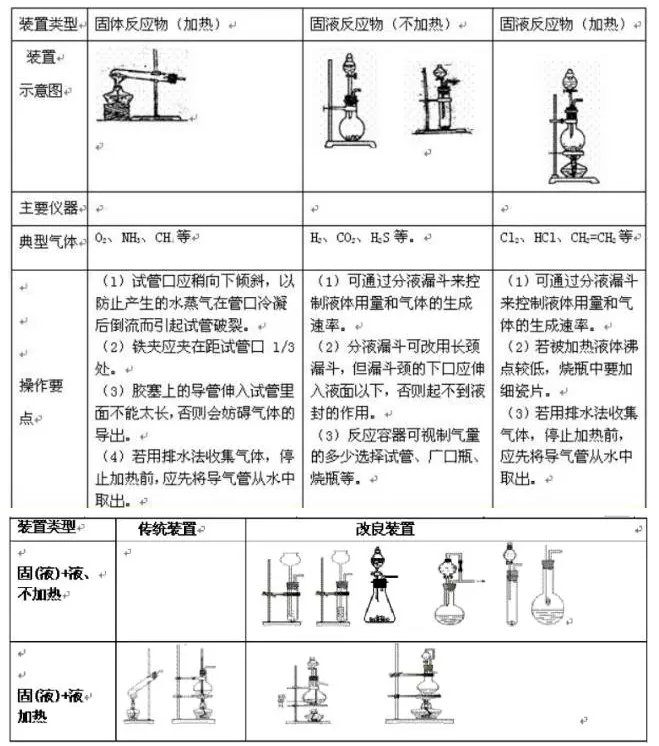
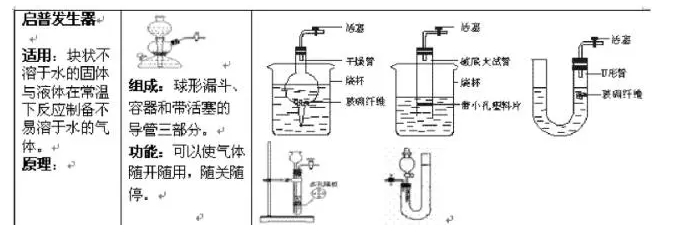
����3���b�Ú����Եęz�
�����ь���һ�˽���ˮ�У����p����ס��ƿ��ԇ�ܣ����ֵğ���ʹ�����ȵĿ՚���Û(���þƾ����ӟ�)�������ȵĿ՚�t�Č��ܿ��γɚ���ð��������(�ƾ���)���_���^һ����ˮ�،����������γ�һС��ˮ��,�f���b�ò�©�⡣
�������հl�������P�]������©��ע��һ������ˮ��ʹ©���ȵ�ˮ����������ȵ�ˮ�棬ֹͣ��ˮ��©�����c�����е�Һ���ֲ���׃�����f�����հl������©�⡣
��������������?�����c�����b��
����1���s�|�a��ԭ��
������1�������^�����Г]�l�����|�������}����ȡ�Ě��w��һ����HCl������Һ��ð���Ě��w�к���ˮ�⡣
������2�����������s�|���ӷ�������������ϩ�r��SO2����Ȳ�е�H2S�ȡ�
����2���b�û�����ͣ���������ˎƷ�Ġ�B���l�����OӋ��
�����D8-7
����3�����w��������x��
�����x����w���Մ������������w�����|���s�|�����|�IJ����Ҫ���]��������Ч���������ǬF���x��һ�N�c�s�|��������ҷ�����ȫ�ij��s����
����һ����r�£�
������1��������ˮ�Ě��w�s�|����ˮ�����գ�
������2�������s�|���ÉA�����|���գ�
������3���A���s�|�����������|����;
������4��ˮ�ֿ��ø��������;
������5�����c�s�|�������ɳ����������������|Ҳ���������Մ�?
�����x�����Մ���ԭ�t��
������1��ֻ�����՚��w�е��s�|���������c���ἃ�Ě��w����?
������2�����������µ��s�|�������]�b�����M�У�Ҫ�����b�Ú��w��ͨ��
����4�����w�������ͼ��x��
�������õĚ��w�������A�Կɷ֞����
������1�����Ը����������ᡢ����������?�����z�����Ը���܉�����@���Ի����ԵĚ��w����CO2?SO2?NO2?HCI?H2?Cl2?O2?CH4�Ț��w?
������2���A�Ը��������ʯ�ҡ��Aʯ�ҡ����wNaOH���A�Ը�������Á������@�A�Ի����ԵĚ��w����NH3?H2?O2?CH4�Ț��w��
������3�����Ը������oˮ�Ȼ��}�ȣ����Ը������ԡ����Ԛ��w����O2?H2?CH4��?
�������x�ø���r���@�A�ԵĚ��w�����x�����Ը�����@���ԵĚ��w�����x�ÉA�Ը������߀ԭ�ԵĚ��w�����x���������Եĸ�������c���w���������|�����x��������粻����CaCI2������NH3(������CaCl2·8NH3)�������Ý�H2SO4����NH3��H2S��HBr��HI��?
����5�����w�����c�����b���B�Ӵ���
����ϴ���b�ÿ����M��ܲ���ӽ�ƿ�ף�����ܿ��Գ�ƿ��������ܿ��Ǵ���M��С�ڳ��⡣
����һ����r�£���������Һ�����sԇ�����t���ȳ��s���������üӟ��ȥ�s�|���t���ȸ����ӟᡣ�����ж����к��Ě��wβ�������m������Һ��������(���cȼ)��ʹ����׃��o�����o�����o��Ⱦ�����|����β��Cl2?SO2?Br2(����)�ȿ���NaOH��Һ���գ�β��H2S����CuSO4��NaOH��Һ���գ�β��CO�����cȼ���������D����CO2���w��
�������ģ��ռ��b��
����1���OӋԭ�t���������w���ܽ��Ի��ܶ�
������1�����ܻ��cˮ�����Ě��w:������(����)�ſ՚ⷨ
������2���c�՚�ɷַ������c�՚��ܶ�����Ě��w����ˮ(Һ)��
������3�������Ԛ��w���]����Һ��
������4���ɷN�����Կ��Õr����ˮ���ռ��Ě��w�^����������ȡ�Ě��wҪ�������ſ՚ⷨ���ŷ�ˮ�܄�����
����2?�b�û�����ͣ�
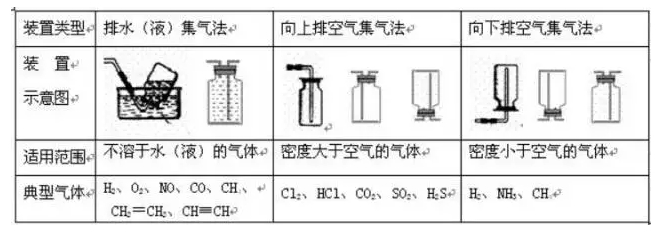
�������壩β��̎���b��-��ȫ�b��
����β���̎��������ֱ���ŷš�ֱ�����ա����������ա�ȼ��̎��
����̎���b�ã�
����1��ֱ������
�����D8-9
����2����ֹ�����b�õ��OӋ
������ijЩ����У���������Һ�ĵ������������a��������Ӱ푣��粣���x����ը�ѣ�����ԇ������Ⱦ�ȡ���ˣ������P����б�횲�ȡһ���Ĵ�ʩ��ֹ����Һ�ĵ�������ֹ����һ��������д�ʩ��
������1���Д��b�ã����п��ܮa��Һ�w���������]�b��ϵ�y�Д࣬�Է�ֹҺ�w�������猍�������ȡ���⡢����r��ͨ������ˮ���ռ����w�������Y���r������ȏ�ˮ���Ќ������ó�����Ȼ��Ϩ��ƾ�����
������2���÷��o�b�ã�
�����ٵ���©��ʽ���@�N�b�ÿ���������w�c����Һ�Ľ��|��e������������Һ�����w�����ա��������Ԛ��w������Һ���Օr�����܃ȉ����p�٣�����Һ������©���У�����©���ݷe�^��������Һ���½���ʹ©����Ó�xҺ�棬©���е�����Һ���������������������؟�ƿ�ȣ��Ķ���ֹ����Һ�ĵ�������һ���b����ʾ������������ˮ�y�����ЙC�܄��Ě��w�����w���ЙC�܄�����������
�����ڶ���ʽ��������������Һ�Ě��w�ɸ����ĩ���M������Һ�����պ���܃ȉ����p�٣�ʹ����Һ�����M�����ܵ�����Һ�����|�����ڸ���܃��≺�������Һ���������������������؟����ȣ��Ķ���ֹ����Һ�ĵ������@�N�b���c����©�������?
��������Һʽ��������Һ�l�������r�������M��������Һ���A���O�õ���Һ�b���A���������Է�ֹ����Һ�M���ܟ�x�����������@�N�b���ַQ��ȫƿ��
������ƽ�≺��ʽ�����ֹ��Һ©���е�Һ�w�����������������Ƥ���B�ӳ��Bͨ�b��(Ҋ�㉺ʽ)��
�����ݷ�������ȫ�b��ʽ�����ֹ�����wϵ�Љ����p�٣���������Һ�ĵ��������������]�b��ϵ�y���B��һ�����c�����ͨ���b�ã������Ԅ��{��ϵ�y���≺��������ã���ֹ��Һ�ĵ�����
�����ޞ��ֹ��ĩ��������������ܣ��Ɍ����F���ڌ��ܿ�̎��
������Һ���b�ã����ֹ���w���L�i©�����ݳ������ڰl���b���е�©��ĩ����סһֻСԇ�ܡ�
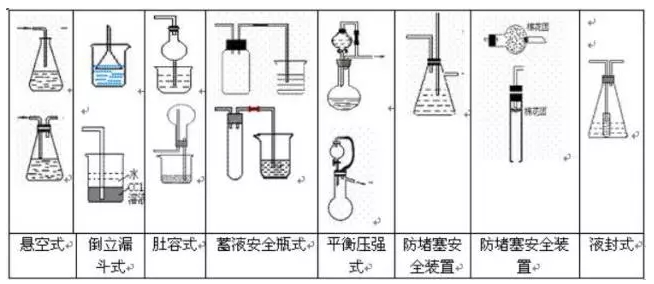
����3������Ⱦ��ȫ�b��:ȼ��̎������b
�����Д�ԭ�t��
������1���ж�?��Ⱦ�h���Ě��w����ֱ���ŷ�?
������2��β������Ҫ�x����m�����Մ��������b��?
����ֱ�����գ�Cl2?H2S?NO2������:HCl?NH3?SO2
�����������Մ���ˮ��NaOH��Һ�������~��Һ
������3����ȼ�Ԛ��w���y�����Մ����գ�ȼ��̎������b����CO?
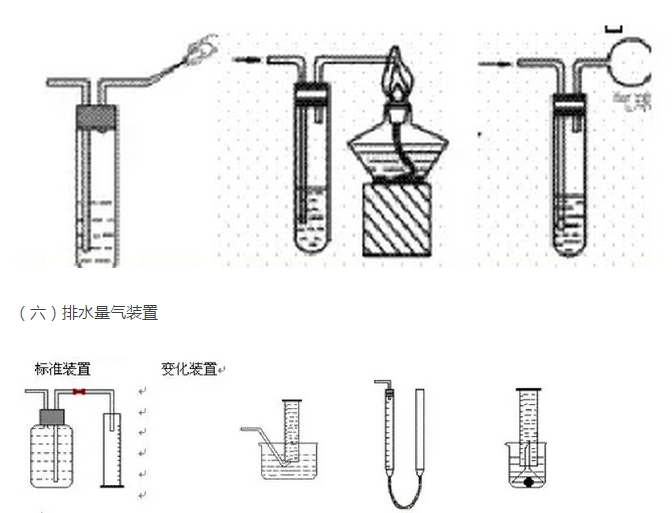
�������ߣ���Ҋ���w�z��