�߿��ЙC���W��݆��������֪�R�c
2019-01-03 21:24:14���þW
����һ������Ĵ��ڡ���;���Y��
����1.����Ĵ����c��;
����(1)����Ĵ���
������������Ȼ�⡢�Ӛ⡢������ú�V�ӵ������Ҫ�ɷ֡��҇�����Ȼ����Ҫ�ֲ����������^�����ס�
����(2)�������Ҫ��;
����������ȼ������ȫȼ������CO2��H2O���ų������ğ�������˼��������ȼ�ϡ���Ȼ����Ӛⶼ��������坍��Դ������߀����������ԭ�ϡ�
����2.����ĽM���c�Y��
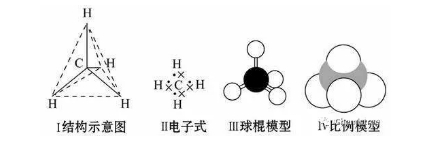
����������������|
����1.������������|
����������һ�N�oɫ���oζ���O�y����ˮ���ܶȱȿ՚�С�Ě��w��
����2.����Ļ��W���|
����(1)�����ȼ������(��������)
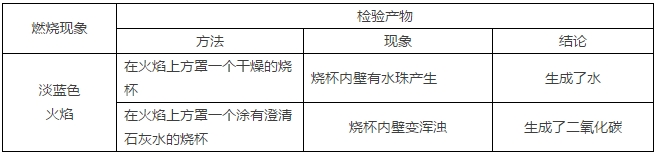
�����ټ����ȼ��
����CH4��2O2→CO2��2H2O
���������ǃ����Ě��wȼ�ϣ�ͨ����r�£�1 mol������ȫȼ�����ɶ�����̼��ˮ���ų�890 kJ����������Լ������Ҫ�ɷֵ���Ȼ�⡢�Ӛ���������坍��Դ��
�����e����
�������cȼ����ǰ��횙z�ȡ��՚��еļ��麬����5%��15.4%(�w�e)�����ȕr�����l����ը����ú�V�е���˹��ը�����Ǽ�����w��ը���l�ġ�
�����ڌ�CH4ͨ������KMnO4��Һ�У�����KMnO4��Һ���ɫ���l��׃����CH4���Ӟ��������w�Y�����Y�����Q��ͨ����r�»��W���|���^������
����(2)�����ȡ������
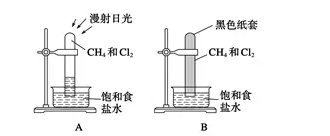
�������F��
����A�b�ã�(1)ԇ�܃Ț��w�ɫ��u׃�\��(2)ԇ�܃ȱ����͠�Һ�γ��F��(3)ԇ�������������F��(4)ԇ�܃�Һ��������(5)ˮ�����й��w������
����B�b��o���@�F��
�������YՓ
����CH4�cCl2�ڹ��Օr���ܰl�����W������
�����ٻ��W��������ʽ
����CH4��Cl2→CH3Cl��HCl��
����CH3Cl��Cl2→CH2Cl2��HCl��
����CH2Cl2��Cl2→CHCl3��HCl��
����CHCl3��Cl2→CCl4��HCl��
������ȡ��������ָ�ЙC������е�ijЩԭ�ӻ�ԭ�ӈF������ԭ�ӻ�ԭ�ӈF������ķ�����CH4��Cl2�������ķNȡ���a�ﶼ������ˮ����һ�ȼ��鳣�����ǚ��w�⣬�������N�����͠�Һ�w��
�����ۆ��}ӑՓ
����a.���Ѽ�������е�һ����ԭ�ӓQ����ԭ��׃��һ�ȼ��飬߀���������w�Y���
�����𰸣���C—H�I�cC—Cl�I���L�Ȳ�ͬ����CH3Cl�������w�Y�����������������w�Y����
����b.CH4�cCl2�l��ȡ�������r���ЙCȡ���a��Ŀ����|�����cCH4�����|�����к��Pϵ��
�����𰸣�����̼Ԫ���غ㣬�ķN�ЙCȡ���a��Ŀ����|�������ڷ�����CH4�����|������
����c.CH3Cl��CCl4ֻ��һ�N�Y�������f��CH4��������̼ԭ�Ӟ����ĵ��������w�Y�������������ε�ƽ��Y���
�����𰸣����ܡ���鲻ՓCH4��������̼ԭ�Ӟ����ĵ��������w�Y����߀�������ε�ƽ��Y����CH3Cl��CCl4��ֻ��һ�N�Y����
����������N
����1.��N�ĽY�����c

����(1)ÿ��̼ԭ���γ�4�����r�I����ԭ��֮�gֻ�Ԇ��I���B��朠̼ԭ�ӵ�ʣ���r�I���c��ԭ�ӽY�ϡ�
����(2)�N������̼ԭ��֮�g����̼̼���I�Y�ϳ�朠ʣ���r�I���c��ԭ�ӽY�ϣ�ʹÿ��̼ԭ�ӵĻ��σr���_��“�”���@�ӵğN�����期N��Ҳ�Q��N�������ͨʽ��CnH2n��2(n≥1��n������)����N�Ŀ��g�Y���У�̼ԭ��(���ڵ���3�r)����һ�lֱ���ϣ�ֱ���N���g�������۾��λ���X�
����2.��N���������|
������N���������|�S��������̼ԭ�Ӕ������࣬��Ҏ���Ե�׃����
����(1)���������B�ɚ�B׃��Һ�B��׃���̑B���ۡ����c��u���ߣ������ܶ���u����
����(2)�����£�̼ԭ�Ӕ�С�ڻ����4�r�������B(�����鳣����Ҳ���B)��
����3.���|�ĽM�ɡ��Y���Q�����|�����|����N�Ļ��W���|�c�������ơ�
����(1)�����ȼ��
����CH3CH2CH3��5O2→3CO2��4H2O��
����(2)���l���£������c�Ț�l��ȡ������(ֻҪ��һ��ȡ��)
����CH3CH3��Cl2→CH3CH2Cl��HCl��














