�߿����W�_�̣����W������Ӌ��֪�R���Y
2018-12-28 21:27:37���þW
����һ���ữ�W����ʽ
����1������
������ʾ���ӷ������|�����ͷ�������Pϵ�Ļ��W����ʽ��
����2�������ữ�W����ʽ��“�岽”
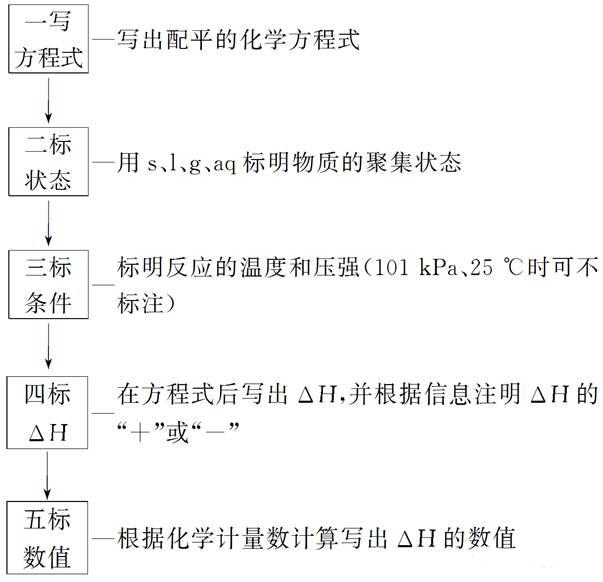
����3���Д��ữ�W����ʽ���`��“�匏”
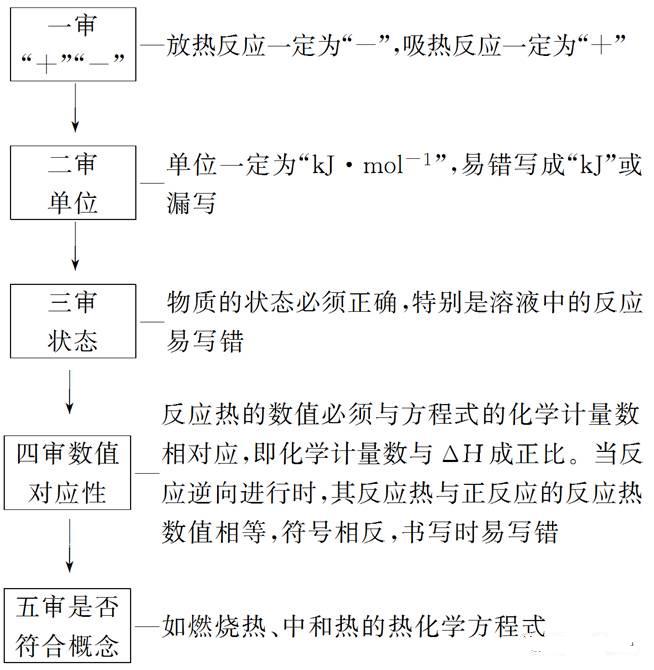
���������w˹����
����1������
�������ܻ��W������һ����֎ײ���ɣ��䷴��������ͬ�ġ������f�����W�����ķ�����ֻ�c�����wϵ��ʼ�B�ͽK�B���P�����c������;���o�P��
���������|A׃��C�������ЃɷN;����

�����t��ΔH1��ΔH2��ΔH3��
����2�����
����������ጷŻ��������l��׃�������|����A�ģ������ܲ��ɷ֣��������|������
����3������
���������M�еú����ķ�����������ֱ�Ӱl���ķ������aƷ����(���и������l��)�ķ������y���@Щ�����ķ����������y����������w˹���ɣ��Ϳ����g�ӵذ������ķ�����Ӌ�������
����4��ע�����
����(1)���ữ�W����ʽ���Ի����ij���r��ΔHҲ�������Ի����ij����
����(2)���ữ�W����ʽ�M�мӜp�\��r��ΔHҲͬ��Ҫ�M�мӜp�\�㣬��Ҫ��“��”��“��”��̖������ΔH����һ�����w�M���\�㡣
����(3)ͨ�^�w˹����Ӌ����^������Ĵ�С�r��ͬ��Ҫ��ΔH����һ�����w��
����(4)���OӋ�ķ����^���г�������ͬһ���|�̡�Һ�������B����D�������|�Ġ�B��“��→Һ→��”׃���r���������֮���şᡣ
����(5)���OӋ�ķ��������M�Еr���䷴�����c�������ķ����ᔵֵ��ȣ���̖�෴��
�����������W�������Ӌ��
����1��������Ӌ�������
����(1)�����ữ�W����ʽӋ�㡣
�����������c����������|�����|���������ȣ���ΔH1��nΔH��
����(2)����������������������Ӌ�㡣
����ΔH��������������ͣ��������������
����(3)�������������������I��Ӌ��
����ΔH����������I�ܺͣ���������I�ܺ�
����(4)�����w˹����Ӌ�㡣
�������ữ�W����ʽ�M���m����“��”��“�p”��׃�κ����^�̵ğ�Ч���M��Ӌ�㡢���^��
����(5)�������|��ȼ���ᔵֵӋ��
����Q(��)��n(��ȼ��)×|ΔH|��
����(6)�����ȟṫʽ�M��Ӌ�㣺Q��cmΔt��
����2��������Ӌ��ij��ý��}����
����(1)�з��̷����Ȍ����ữ�W����ʽ���ٸ����ữ�W����ʽ���w�F�����|�c�������g���Pϵֱ�����㷴���ᡣ
����(2)���㷨�������ữ�W����ʽ����ʾ�����ğ�Ч���c�����ȼ���ų��ğ��������¹�����ɷֵı�����
�����˷���Ҫ�����ڽ���x���}�������}�o��Ϣ�ҳ����·���������Դ��������ҳ��𰸣��˷����}���١����㡣














