�߿����W�_�̣��}�ˮ�⼰��Ҏ(gu��)��֪�R���Y
2018-12-25 21:30:57���þW(w��ng)
����1�����|
������ˮ��Һ���}��x�������x��(���A����x�ӻ��������x��)�Y��ˮ��x����OH����H�����Ɖ���ˮ����xƽ�⣬���M��ˮ����x��ʹ��Һ�@ʾ��ͬ�����ԡ��A�Ի����ԡ�

����4��Ӱ��}�ˮ�������
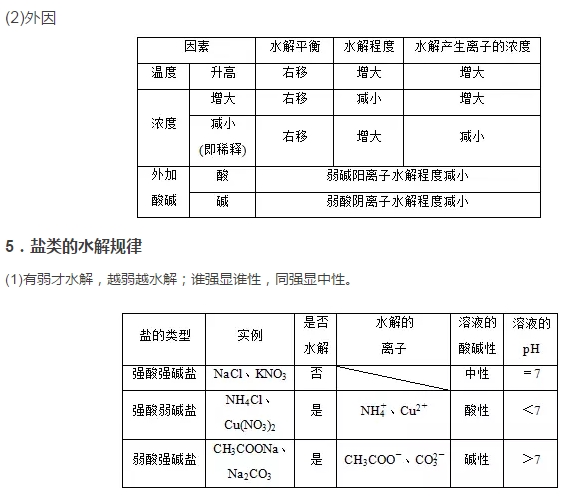
����(1)����
����������x�ӡ����A��x�ӌ������ᡢ�AԽ������Խ�װl(f��)��ˮ�⡣